Введение
В Российской Федерации распространенность сердечно-сосудистых заболеваний (ССЗ) достигла масштаба эпидемии. Пациенты с кардиологическими нарушениями преобладают на приеме не только у терапевтов, но и у врачей других специальностей. О каких больных из этой группы думает гастроэнтеролог? Конечно, речь идет о тех из них, кто принимает антитромбоцитарные препараты и нестероидные противовоспалительные средства. Согласно современным рекомендациям, с целью профилактики сердечно-сосудистых осложнений пациентам с ишемической болезнью сердца (ИБС) показано применение антитромбоцитарных препаратов (аспирин, клопидогрел, тиклопидин). Между тем для купирования боли, обусловленной сопутствующими заболеваниями (артриты, костно-мышечная патология и др.), больные зачастую бесконтрольно принимают множество самых разнообразных нестероидных противовоспалительных средств (НПВС).
Учитывая повсеместное назначение антитромбоцитарных препаратов для продолжительного приема, вопросы безопасности данной терапии становятся весьма актуальными. Использование антитромбоцитарных препаратов и НПВС ассоциируется с повреждением слизистой верхних отделов желудочно-кишечного тракта (ЖКТ), включая эрозивно-язвенные поражения, желудочно-кишечные кровотечения и перфорацию.
У лиц, регулярно принимающих НПВС, в 25% случаев возникает язвенное поражение ЖКТ, а частота развития кровотечений и перфораций составляет 2—4%.
Частота крупных желудочно-кишечных кровотечений при применении аспирина составляет от1,8 до 3,7%, а при приеме двойной антитромбоцитарной терапии (аспирин и клопидогрел) от 3,0 до 4,9% в зависимости от дозы аспирина (75—325 мг). Развитие кровотечений верхних отделов ЖКТ на фоне малых доз аспирина составляет 0,5% в год (относительный риск (ОР) по сравнению с плацебо составляет 2,07; 95% ДИ 2,61—2,66). В семь раз увеличивается риск развития желудочно-кишечных кровотечений на фоне комбинации клопидогрела и аспирина (отношение шансов (ОШ): 7,4; 95% ДИ 3,5—15) по сравнению с монотерапией аспирином.
Оценка риска нежелательных эффектов НПВС и антитромбоцитарных препаратов на желудочно-кишечный тракт
Факторы риска негативного действия антитромбоцитарных средств и НПВС на ЖКТ сформулированы в рекомендациях, приведенных в American College of Gastroenterology, по предотвращению осложнений гастропатии, индуцированной НПВП. Выделены градации по степени риска негативного действия НПВС на ЖКТ: высокий, умеренный и низкий риск. Кроме того, наличие инфекции пилорического хеликобактера служит независимым и дополнительным фактором риска, который необходимо рассматривать отдельно (см. таблицу).
Исходя из данных рекомендаций, многие пациенты кардиологического профиля даже при отсутствии язвенного анамнеза относятся к группе высокого риска по развитию желудочно-кишечных осложнений при приеме НПВС и антитромбоцитарных средств.
НПВС и аспирин чаще всего принимают пациенты старше 60 лет, из-за своего возраста сразу оказываясь в группе высокого риска. Повышенная частота развития желудочно-кишечного кровотечения и перфорации в пожилом возрасте по сравнению с более молодыми лицами объясняется возрастным уменьшением эндогенного синтеза простагландинов. Кроме того, доказано, что в пожилом возрасте непосредственно страдают защитные механизмы гастродуоденальной слизистой оболочки: снижаются кровоток, синтез муцина и секреция бикарбонатов. Старший возраст негативно влияет на течение язвенной болезни.
Более того, большинство пожилых пациентов вынуждено длительно принимать аспирин, клопидогрел, двойную, а иногда и тройную антитромбоцитарную терапию (аспирин, клопидогрел, варфарин). Не редкость и параллельный прием НПВС.
Ингибиторы протонной помпы: целесообразность профилактического назначения
Врачам-клиницистам приходится оценивать соотношение риск/польза и балансировать между положительными эффектами антитромбоцитарной терапии в предотвращении сердечно-сосудистых нарушений и соблюдением древнего врачебного принципа «не навреди».
Очевидно, что необходимо проводить профилактику НПВС-гастропатии и желудочно-кишечных кровотечений на фоне антитромбоцитарной терапии. Действенным способом снижения высокого риска желудочно-кишечных осложнений, обусловленного антитромбоцитарными препаратами, может служить дополнительное назначение ингибиторов протонной помпы (ИПП). Согласно международным рекомендациям, ИПП служат препаратами выбора для терапии и профилактики НПВС- индуцированных гастропатий и поражений ЖКТ на фоне антитромбоцитарной терапии.
Эффективность такого подхода продемонстрирована при лечении НПВС, при монотерапии аспирином и при двойной антитромбоцитарной терапии аспирином и клопидогрелом.
Так, риск язвенного поражения желудка и двенадцатиперстной кишки, индуцированного прие¬мом НПВС, снижается на фоне применения ИПП (ОР 0,37; 95% ДИ 0,27—0,51).
В исследовании А. Lanas и соавт. с участием 2777 пациентов с кровотечениями из верхних отделов ЖКТ и 5532 из группы контроля прием ИПП ассоциировался со снижением риска кровотечений как для принимающих низкие дозы аспирина (ОШ 0,32; 95% ДИ 0,22—0,51), так и для принимающих клопидогрел (ОШ 0,19; 95% ДИ 0,07—0,49).
У пациентов с ИБС, получающих двойную антитромбоцитарную терапию аспирином и клопидогрелом, профилактическое назначение ИПП приводит к уменьшению частоты кровотечений из верхних отделов ЖКТ. Такие результаты были получены в ходе крупного плацебо-контролируемого рандомизированного исследования COGENT с участием больных в количестве 3761 человека, нуждающихся в длительной двойной антитромбоцитарной терапии (перенесших острый коронарный синдром или коронарное стентирование).
Добавление омепразола в дозе 20 мг в сутки к комбинации аспирина и клопидогрела сопровождалось достоверным уменьшением риска желудочнокишечных кровотечений на 45%. В группе больных, получавших ИПП, реже отмечались как любые желудочно-кишечные нарушения (ОР=0,34; 95% ДИ 0,18—0,63; р <0,001), так и явные кровотечения из верхних отделов ЖКТ (ОР=0,13; 95% ДИ 0,03—0,56; р=0,001) по сравнению с группой, получавшей плацебо. В исследовании COGENT продемонстрировано, что эффективность антитромбоцитарного лечения не снизилась при добавлении ИПП. Не отмечено и статистически значимого увеличения риска сердечно-сосудистых событий на фоне добавления ИПП к антитромбоцитарной терапии. В общей сложности сердечно-сосудистые события зарегистрированы у 4,9% пациентов из группы, получавшей ИПП, и 5,7% из группы, получавшей плацебо (ОШ=0,99; 95% ДИ 0,68—1,44; р=0,96). Однако к заявленным результатам следует относиться критически, поскольку данное исследование было прекращено досрочно по причинам финансового характера.
ЖЕЛУДОЧНО-КИШЕЧНЫЕ ОСЛОЖНЕНИЯ И АНТИТРОМБОЦИТАРНЫЕ ПРЕПАРАТЫ
Ингибиторы протонной помпы при приеме антитромбоцитарных средств: кому и когда?
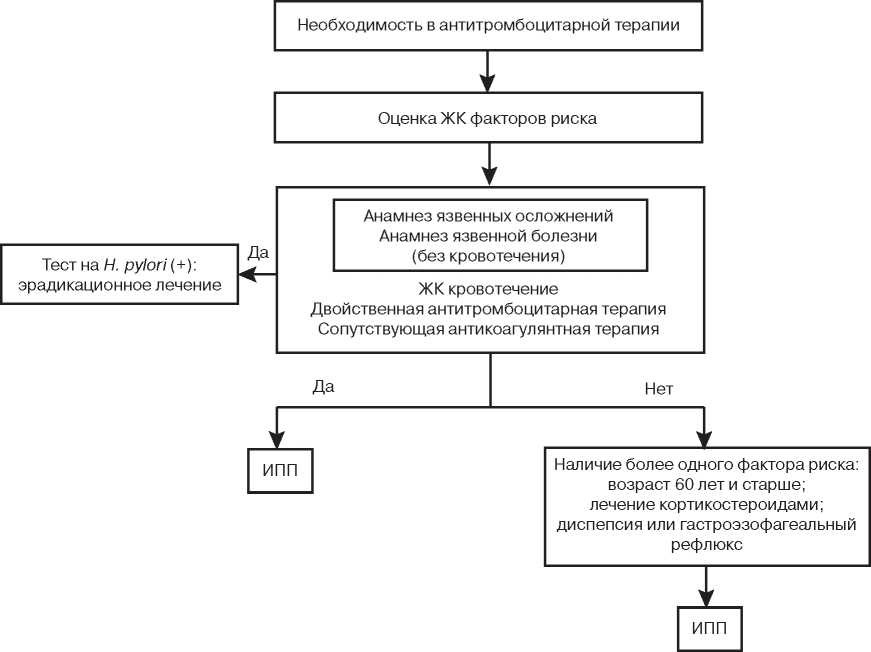
При отборе пациентов для дополнительной терапии ИПП необходимо оценить факторы риска и сопутствующие заболевания (см. таблицу). Возраст, использование варфарина, стероидов, НПВС или инфекция Н. pylori увеличивают риск желудочнокишечных кровотечений на фоне антитромбоцитарной терапии. Для клинического применения разработан алгоритм снижения риска негативного действия антитромбоцитарных средств на ЖКТ путем применения ИПП (см. рисунок).
Как избежать лекарственного взаимодействия
В настоящее время в медицинском мире активно обсуждается вопрос о взаимодействии и безопасности сочетания клопидогрела с ИПП (особенно с омепразолом), так как ИПП потенциально способны уменьшить количество активного метаболита клопидогрела и выраженность его антитромбоцитарного действия. Определенный генетический полиморфизм, высокая вероятность лекарственных взаимодействий в системе цитохрома P-450 при добавлении ИПП может приводить к изменениям антитромбоцитарной эффективности клопидогрела ИПП.
Клопидогрел — пролекарство, которое при помощи системы цитохрома Р-450 в печени трансформируется в активный метаболит. Активный метаболит клопидогрела селективно и необратимо блокирует связывание АДФ с рецепторами тромбоцитов типа P2Y12, что в свою очередь блокирует их активацию через 11Ь/111а комплекс. Активация клопидогрела происходит в два этапа. Вначале он подвергается окислительной биотрансформации в печени с участием изоферментов СУР2С19, СУР1А2 и СУР2В6, превращаясь в 2-оксо-клопидогрел. Вто¬рым этапом является гидролизация 2-оксо-клопи- догрела в активный метаболит клопидогрела при помощи изоферментов СУРЗА, СУР2В6, СУР2С9, СУР2С19.
Метаболизм клопидогрела и 2-оксо-клопидо- грела в большой степени зависит от индукции или ингибирования СУР2С19, что обусловлено влиянием различных лекарственных препаратов, а также индивидуального генетического полиморфизма.
Метаболизм ИПП, так же как и клопидогрела, происходит в системе цитохрома Р-450, преимущественно с участием СУР2С19 и в меньшей степени — СУР3А4.
Применение ИПП может ингибировать превращение клопидогрела в активный метаболит за счет влияния на СУР2С19, приводя к ослаблению его антитромбоцитарной активности. Риск отсутствия эффективности лекарственного препарата возрастает, когда его концентрация зависит от изменчивой активности единственного пути метаболизма. Такой высокий фармакокинетический риск обнаружен у клопидогрела.
Другим объяснением влияния ИПП на активность клопидогрела может служить изменение внутрижелудочного рН на фоне приема ИПП, что меняет всасывание клопидогрела. ИПП блокируют протонную помпу париетальных клеток желудка, и восстановление внутрижелудочного рН возможно лишь с прекращением длительного терапевтического эффекта ИПП, через 12—24 ч.
Кроме того, фармакокинетическое и антитромбоцитарное тестирование активного метаболита клопидогрела показало, что концентрация и антитромбоцитарные эффекты препарата различаются в зависимости от генетического полиморфизма фермента СУР2С19. Аллель СУР2С19*1 обусловливает полностью функционирующий метаболизм клопидогрела. Аллели СУР2С19*2 и *3 не обеспечивают эффективного метаболизма клопидогрела. У пациентов с двумя аллелями сниженной активности (гомозиготы) наблюдается медленная метаболизация клопидогрела. Определенный генетический полиморфизм может приводить к увеличению сердечнососудистого риска на 50% и к трехкратному увеличению риска тромбоза стентов у больных, получающих клопидогрел.
Клиническая эффективность совместного применения ингибиторов протонной помпы и клопидогрела
В декабре 2010 г. опубликован консенсус American College of Cardiology и American College of Gastroenterology по поводу совместного примене¬ния тиенопиридинов (клопидогрел, прасугрел) и ИПП, в котором подробно освещены вопросы изменения эффективности клопидогрела на фоне приема ИПП. Результаты клинических исследований, представленные в данных рекомендациях, разнятся — от статистически недостоверного влияния ИПП на увеличение риска сердечно-сосудистых нарушений до значимой связи между приемом ИПП и сердечно-сосудистым риском.
В ретроспективном когортном исследовании M. O’Donoghue и соавт. с участием 13 608 пациентов, принимавших клопидогрел или прасугрел после стентирования, не выявлено влияния ИПП на увеличение смертности по причине сердечно-сосудистой патологии, инфаркта миокарда или инсульта (ОР для клопидогрела 0,94; 95% ДИ 0,80—1,11). Не продемонстрировано различий между видами ИПП, включая омепразол (n=1675), лансопразол ( n=441), эзомпразол ( n=613) и пантопразол ( n=1844). ИПП не увеличивали частоту сердечнососудистых эпизодов даже у пациентов — «медленных метаболизаторов», которые имели сниженную функцию аллеля CYP2C19. В исследовании CREDO (Clopidogrel for Reduction of Events During Observation) прием ИПП ассоциировался с увеличением частоты случаев сердечно-сосудистых нарушений как у пациентов на фоне применения клопидогрела, так и без него.
Лишь одно рандомизированное клиническое исследование, упомянутое выше COGENT, было посвящено взаимосвязи между клопидогрелом и ИПП. Доказано отсутствие влияния ИПП на увеличение сердечно-сосудистого риска при параллельном статистически достоверном снижении риска желудочно-кишечных осложнений.
Возможности пантопразола в профилактике желудочно-кишечных осложнений на фоне антитромбоцитарных препаратов
На сегодняшний день последние рекомендации (ACCF/ACG/AHA 2010 Expert Consensus Document on the Concomitant Use of Proton Pump Inhibitors and Thienopyridines) не указывают на приоритетное назначение того или иного ИПП на фоне антитромбоцитарной терапии. Ретроспективное исследование (W. Ray, 2010) с участием 20 596 больных не показало значимого влияния ни одного из используемых ИПП (эзомепразол, лансопразол, омепразол, рабепразол, пантопразол) на увеличение частоты сердечно-сосудистых эпизодов .
ЖЕЛУДОЧНО-КИШЕЧНЫЕ ОСЛОЖНЕНИЯ И АНТИТРОМБОЦИТАРНЫЕ ПРЕПАРАТЫ
Последний метаанализ S. Shukla и S. Guba не позволяет сделать вывод о том, что ИПП снижают активность клопидогрела. Но все же одновременно с клопидогрелом авторы рекомендуют назначать не омепразол, а пантопразол или рабепразол, поскольку последние не влияют на систему цитохрома 2C19.
Исходя из знаний фармакокинетических свойств ИПП и их влияния на систему цитохрома Р-450, можно говорить о преимуществах назначения пантопразола (Контролок, Никомед) пациентам с сердечно-сосудистой патологией, получающим антитромбоцитарные препараты.
Пантопразол имеет более низкую афинность к печеночной системе цитохрома Р-450, не влияет на ее активность и не дает клинически значимых реакций со многими лекарственными препаратами, в том числе с антитромбоцитарными средствами и НПВС. Это значительно расширяет область его применения, поскольку пантопразол больше подходит для назначения совместно с другими медикаментами, позволяя с большей уверенностью предположить, что их действие не изменится в сторону усиления, ослабления или извращения. В результате действие других лекарственных препаратов, метабо-лизирующихся с участием ферментных систем данного цитохрома, не ослабляется, что особенно актуально у пожилых больных с кардиологическими проблемами, вынужденных одновременно принимать несколько препаратов.
Пантопразол в незначительной степени подвергается метаболизму первого прохождения и имеет постоянную величину биодоступности после первого приема. Пантопразол — единственный ИПП, связывающийся с цистеином протонного насоса в положении 822. Предполагается, что цистеин 822 обеспечивает устойчивость связи и длительность ингибиции протонной помпы и кислотной продукции. Поэтому пантопразол характеризуется более продолжительным кислотоснижающим эффектом.
При более широком диапазоне рН пантопразол накапливается в париетальных клетках и вступает во взаимодействие с тиольной группой протонной помпы. Будучи более стабильным соединением, пантопразол с меньшей вероятностью прореагирует с тиольными группами белков вне париетальной клетки, что позволяет рассчитывать на его прогно-зируемые фармакокинетические свойства.
Если говорить о лекарственном взаимодействии между антитромбоцитарными препаратами и пантопразолом, то последний обладает низкой способностью вступать в данное межлекарственное взаимодействие. Это связано с меньшей афинностью пантопразола по сравнению с другими ИПП к изоферментам CYP2C19 и CYP3A4.
В отличие от большинства продуктов, образующихся в фазе I биотрансформации других ИПП, первоначальный метаболит пантопразола 4-гидроксипантопразол, образуемый системой CYP, очень быстро покидает систему цитохрома Р-450, в результате чего нивелируется возможность конкуренции с разными лекарственными препаратами на уровне изоферментов CYP. 4-гидроксипантопразол затем биотрансформируется вторично (фаза II) посредством конъюгации с сульфатом в цитозоле. Эту реакцию конъюгации часто расценивают как причину более низкой способности пантопразола вступать в межлекарственные взаимодействия.
Если говорить о препаратах пантопразола, то препаратом-лидером служит оригинальный пантопразол — Контролок (Никомед). Молекула оригинального пантопразола имеет уникальную двойную оболочку, которая защищает действующее вещество от агрессивной кислой среды желудка и позволяет ему всасываться в кишечнике. Контролок обладает такими свойствами, как необратимая и полная блокада протонных помп, линейная биодоступность (одинаковая для каждого дня терапии), независимость от приема пищи, совместимость с другими лекарственными средствами, в том числе с антитромбоцитарными препаратами. Таким образом, Контролок (Никомед) является приоритетным препаратом для дополнительного назначения кардиологическим пациентам с кардиологическими проблемами из группы риска по развитию желудочно-кишечных осложнений, вынужденных принимать антитромбоцитарные препараты. Это обусловлено минимальными межлекар-ственными взаимодействиями, влиянием пантопразола на систему цитохрома Р-450 и продолжитель¬ным, устойчивым кислотоснижающим эффектом.
Заключение
Необходимость длительного приема антитром- боцитарных препаратов связана с повышением риска развития поражения желудочно-кишечного тракта. Дополнительный профилактический прием ИПП достоверно снижает риск желудочно-кишечных кровотечений, но вызывает противоречивые мнения по поводу ослабления антитромбоцитарной эффективности и по проблеме лекарственного взаимодействия. Метаболизм как ИПП, так и антитромбоцитарных средств изоферментами CYP печеночной системы цитохрома Р-450, а также индивидуальный генетический полиморфизм определяют эффективность и безопасность данной комбинации. Среди ИПП оригинальный препарат пантопразола (Контролок, Никомед) обладает наименьшей способностью межлекарственного взаимодействия и может служить препаратом выбора при на¬значении пациентам кардиологического профиля с высоким риском развития желудочно-кишечных осложнений, вынужденным постоянно получать антитромбоцитарную терапию.
Список литературы
- Рекомендации по антитромботической терапии у больных со стабильными проявлениями атеросклероза (подготовлены Е.П. Панченко с участием Е.С. Кропачевой). Атеротромбоз 2009; 1 (2): 38—54.
- Cryer B., Feldman М. Effects of nonsteroidal anti-inflammatory drugs on endogenous gastrointestinal prostaglandins and therapeutic strate¬gies for prevention and treatment of nonsteroidal, anti-inflammatory drug-induced damage. Archive Intern Med 1992; 152: 1145—1155.
- Soll A.H., Weinstein WM., Kurata J., McCarthy D. Nonsteroidal anti¬inflammatory drugs and peptic ulcer disease. Ann Intern Med 1991; 114: 307—319.
- Laine L. Nonsteroidal anti-inflammatory drug gastropathy. Gastroin¬ test Endosc Clin North Am 1996; 6: 489—404.
- Bombardier C., Laine L., Reicin A., Shapiro D., Burgos-Vargas R, Davis B. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis. VIGOR study group. N Engl J Med 2000; 343: 1520—1528.
- Peters R., Mehta S., Fox K., Zhao F, Lewis B.S., Kopecky S.L., Diaz R., CommerfordP.J., Valentin V., Yusuf S. Effects of aspirin dose when used alone or in combination with clopidogrel in patients with acute coro¬nary syndromes: observations from the Clopidogrel in Unstable angina to prevent Recurrent Events (CURE) study. Circulation 2003; 108 (14): 1682—1687.
- Laine L. Review article: gastrointestinal bleeding with low-dose aspi¬ rin — what’s the risk? Aliment Pharmacol Ther 2006; 24: 897—908.









